Molekyler med forskellige atomer
 Grundbeskrivelse
Grundbeskrivelse
Mange kemiske forbindelser er opbygget af molekyler med to eller flere atomer af forskellige grundstoffer. Et velkendt eksempel er vand, der består af ilt (oxygen), O og brint (hydrogen), H.
Et brintatom har én elektron og et iltatom har otte elektroner udenom kernen. I den simpleste atommodel er to af iltatomets otte elektroner i den inderste elektronskal, mens seks er i den yderste skal.
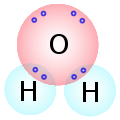
Elektronkonfiguration i et vandmolekyle (Apostoloff, Wikimedia Commons).
Iltatomet stræber efter at have otte elektroner i den yderste skal. I et brintatom befinder den enlige elektron sig i den inderste skal. Her er der plads til to elektroner, så et brintatom stræber efter at have to elektroner.
I et vandmolekyle er der hægtet to brintatomer på iltatomet. Hvert af dem har en elektron fælles med iltatomet. De fælles elektroner 'tæller med' i begge atomers elektronstruktur. På den måde når alle tre atomer op på de eftertragtede otte eller to elektroner.
De to par fælles elektroner danner to kovalente bindinger, der holder molekylet sammen.
 Uddybende beskrivelse
Uddybende beskrivelse
I et iltatom er der 8 elektroner omkring kernen. Der er to i 1s-orbitalen - den inderste skal. Brintatomets ene elektron er ligeledes i 1s-orbitalen.
I iltatomets yderste skal er der to i 2s-orbitalen og i en af de tre 2p-orbitaler. De sidste to elektoner er i hver sin 2p-orbital. Der er på den måde to 2p-orbitaler i iltatomet, der hver mangler en elektron for at være fyldt. Hvert af de to brintatomer mangler en elektron for at få sin 1s-orbital fyldt.
Yderst i vandmolekylet er der otte elektroner, hvor de fire er to par, der er fælles. De fælles elektroner hører til iltatomets halvfulde 2p-orbitaler og hvert af de to brintatomer. De sidste fire stammer fra iltatomets 2s- og en af 2p-orbitalerne, der er fyldt og ikke danner par med brintatomerne. De fire elektronpar vil på grund af den elektriske frastødning søge at sidde så langt fra hinanden som muligt.
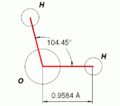
Vinkel og afstand mellem atomerne i et vandmolekyle (Dysprosia, Wikimedia Commons)
Det betyder, at det opsøger en tetraederformet konfiguration, hvor vinklen fra midten af iltatomet ud til hver elektronpar bliver omkring 109°. De elektronpar, hvor der ikke sidder brintatomer, er lidt tættere på kernen og derfor også på hinanden. Derfor frastøder de hinanden en smule kraftigere end dem, der hænger sammen med brintatomerne. De bliver skubbet lidt længere fra hinanden, og derfor bliver brintatomerne skubbet lidt sammen. Brintatomerne kommer på den måde til at danne en vinkel på 104.45°.
På den måde kommer vandmolekylet til at have de to brintatomer 'i den ene ende' og iltatomet 'i den anden ende'. Det gør vandmolekylet til et polært molekyle - det er positivt elektrisk ladet der, hvor brintatomerne er, og negativt i den ende, hvor iltatomet er.
De polære molekyler gør vand til et stof med mange særprægede egenskaber. De polære molekyler tiltrækker hinanden, så vand har så at sige bedre sammenhængskraft end mange andre ellers lignende stoffer.
Model af vandmolekyle (Coopkev2, Wkimedia Commons).
Det betyder, at vands kogepunkt på 100°C er meget højere end det 'burde' være ud fra molekylernes masse alene. Forskellen er næsten 200°C.
I en vandoverflade giver vandmolekylernes indbyrdes tiltrækning anledning til overfladespændingen. Den giver vandoverfladen en lille, men mærkbar mekanisk styrke, så den f.eks. kan bære insekter, der så kan gå på vandet.
De polære molekyler gør det nemt at opløse stoffer, der selv har polære molekyler, f.eks. sukker, i vand. Ligeledes kan en væske som alkohol, der også har polære molekyler, blandes med vand i alle forhold. Derimod kan vand ikke blandes homogent med stoffer, der består af ikke-polære molekyler som f.eks. fedt. Det er derfor olie flyder ovenpå vand i stedet for, at de to væsker blandes.
Michael Quaade
Vælg en kategori