Elektrisk element
 Grundbeskrivelse
Grundbeskrivelse
Et elektrisk element alternativt en akkumulator er en måde at have lager af elektrisk energi. Energien opbevares normalt i form af kemisk energi, som så anvendes til skabelse af en elektrisk strøm ved brugen af elementet. Dette sker normalt når man skaber et lukket kredsløb til elementets poler. Flere elementer sat sammen kaldes et batteri!
Et element består i princippet af to elektroder, en positiv og en negativ. De to elektroder er adskilt af en elektrolyt. En elektrolyt er en væske, der kan lede elektrisk strøm (der kan være tale om pastaer eller faste stoffer).
Alessandro Volta fra Italien var den første, der fremstillede et brugbart element, som kunne afgive elektrisk energi i længere tid. Voltas element bestod af en kobberskive og en zinkskive adskilt af en papskive vædet med en saltopløsning. Volta konstruerede et batteri ved at stable flere elementer i serie oven på hinanden i en Voltasøjle. Kobberskiven er den positive og zinkskiven den negative elektrode.
Et brunstensbatteri består af et zinkhylster, fyldt med en elektrolyt af manganoxid, zinkchlorid eller amoniumchlorid, som er gjort tyktflydende med vand og hvedemel. Midt i elektrolytten er der en kulstang, der er den positive elektrode.
I de genopladelige batterier er nikkel eller lithium tit den ene elektrode og den anden er cadmium, et metalhydrid eller forskellige lithiumforbindelser.
 Uddybende beskrivelse
Uddybende beskrivelse
Normalt består et element af to forskellige metaller adskilt af en opløsning som indeholder ioner fx Na+ og Cl-
Volta fra Italien var den første, der fremstillede et brugbart element, som kunne afgive elektrisk energi i længere tid. Voltas element bestod af kobber og zink adskilt af stof vædet i en saltopløsning. Volta konstruerede et batteri ved at stable flere elementer i serie oven på hinanden i en Voltasøjle. Kobberelektroden er den positive og zinkelektroden den negative.
Den elektriske strøm går fra den positive kobberelektrode til den negative zinkelektrode, har man vedtaget for mange år siden. I dag ved vi, at den elektriske strøm i en ledning i virkeligheden er elektroner, der bevæger fra den negative elektrode til den positive. Den spændingsforskel, der opstår i et element, afhænger af, hvilke metaller der anvendes, og jo længere væk metallerne står fra hinanden i spændingsrækken, jo større spændingsforskel er der. Typisk vil spændingsforskellen være omkring 0,3 volt, hvis de to metaller står tæt op ad hinanden i spændingstrækken.
Et bilbatteri består – før opladning - af flere elementer af blyplader adskilt af fortyndet svovlsyre. Når blypladerne sættes i svovlsyren reagerer overfladen med sulfat-ionen, så der dannes et overfladelag af blysulfat. Når batteriet oplades, dannes der er overfladelag af blyoxid på den ene blyplade, mens den anden blyplade får en overflade af rent bly. Dermed er der to forskellige elektroder, og dermed opstår der også en spændingsforskel. Når elementet er afladt, har begge elektroder et overfladelag af blysulfat.
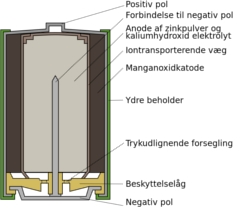
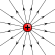
Alkalisk element (Tympanus, Wikimedia Commons).
I dag er brunstensbatterier mere eller mindre fortrængt af alkaliske batterier, der har større kapacitet. Her er elektrolytten alkalisk (basisk) og består af kaliumhydroxid.
I de genopladelige batterier er det tit nikkel, der anvendes som elektrode, også sammen med cadmium eller et metalhydrid. En anden form for genopladelige batterier er lithium-ion-batterier, som indeholder metallet lithium og flere forskellige lithiumforbindelser. En celle kan have en udgangsspænding imellem 1,5 V og 3,8 V afhængigt af de indgående stoffer. Mange har god lagerbestandighed.
Desværre er der endnu ikke opfundet det helt gode batteri til opbevaring af energi.
Erland Andersen og Chritian Petresch
Vælg en kategori